在老年患者中,DLBCL 是最常见的恶性淋巴瘤。R-CHOP 是目前标准的一线治疗,但约 40% 老年患者对标准剂量不能耐受,因此对于这类患者的临床管理仍具有很大挑战。正在进行的第 25 届欧洲血液学年会(European Hematology Association,EHA)已发表了关于老年 DLBCL 患者的治疗现状报道,本文为大家带来最新研究速递。
1. 单中心回顾性研究:>80 岁老年 DLBCL 患者的 10 年随访结果
【研究目的】
DLBCL 患者的预后风险与年龄密切相关,然而在真实世界中,年老患者的治疗结果与临床试验不一致。英国诺福克和诺维奇大学医院对诊断时大于 80 岁的 DLBCL 患者,进行了为期 10 年的人口统计学和治疗结果的随访研究。
【研究方法】
查阅医院电子病历记录,在 2009 年 1 月 1 日至 2019 年 12 月 31 日之间,有 156 位诊断时年龄在 80 岁以上的 DLBCL 患者。通过收集患者的人口统计学数据(包括年龄,身体表现评分,疾病分期,化疗、放疗)及各自治疗结果。
【研究结果】
诊断时患者的中位年龄为 83 岁(范围 80-95),中位随访时间为 5.2 年。在分析时,将近四分之一的患者仍然存活,占 24.3%(38/156),中位总生存期为 0.68 年。 47%(73/156)的患者接受了强化化疗(R-CHOP、R-miniCHOP 和 R-GEMCVP),其他患者接受非强化化疗(口服苯丁酸氮芥和/或依托泊苷)或支持治疗。
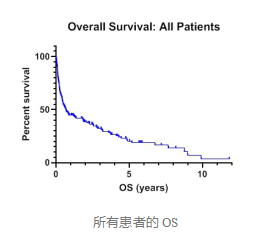
研究结果发现,选择强化化疗的患者中位 OS 为 3.08 年,相比之下,采用非强化化疗方案(0.57 年)或最佳支持/姑息治疗(0.2 年)的患者,中位 OS 明显偏低。在使用的 3 种强化化疗方案之间,中位 OS 无统计学差异,但观察到蒽环类药物有毒性减少趋势。
【研究结论】
接受强化化疗方案治疗患者的生存期高于非强化化疗方案治疗患者,但是治疗决策取决于患者的身体状况,合并症,患者和家庭的意愿。因此,需要对虚弱和老年 DLBCL 患者进行前瞻性试验,以更好地选择最佳治疗策略。
2. 老年综合评估可以有效指导老年 DLBCL 患者治疗
【研究目的】
最近有研究表明老年综合评估(Comprehensive Geriatric Assessment,CGA)可以识别适合标准剂量 R-CHOP 治疗的老年 DLBCL 患者。目前在中国还没有关于此类研究的报道,该前瞻性研究评估 CGA 驱动治疗老年 DLBCL 患者的耐受性和有效性。
【研究方法】
研究纳入 78 例 ≥ 60 岁 DLBCL 患者,分为健康(fit)、不健康 (unfit) 或虚弱 (frail) 组,其中健康组患者接受标准剂量 R-CHOP 治疗,后两组患者接受减量或减药物治疗。研究评估三组的 ORR、OS、PFS 和毒性。
CGA 分类标准 | |||
健康组 (fit) | 不健康组 (unfit) | 体弱组 (frail) | |
ADL | 6 | 5 | <5 |
IADL | 且 8 | 或 6~7 | 或 <6 |
MCIRS-G | 且无 3~4 等级并发症(且 <5 个等级 2 并发症) | 或无 3~4 等级并发症(且 5~8 个等级 2 并发症) | 或 ≥ 1 个 3~4 等级并发症(或 >8 个等级 2 并发症) |
年龄 | 且 <80 岁 | 或 ≥ 80 岁健康患者 | 或 ≥ 80 岁不健康患者 |
ADL:activities of daily living,日常活动能力
IADL:工具性 ADL
MCIRS-G:改良老年疾病累计评分
【研究结果】
根据 CGA,将患者分为健康组:45 例患者(57.5%),不健康组:5 例(6.4%),体弱组:28 例(35.9%)。ORR 为 82.1%(64/78),包括 55 名患者(70.6%)获得 CR,9 名患者(11.5%)获得 PR。健康组和另外 2 组的 ORR 分别为 97.8% 和 60.6%。总共有 26(33.3%)例患者(10/45 [22.2%] 健康组和 16/33 [48.5%] 不健康+体弱)显示疾病进展或复发。中位随访时间为 18 个月(范围:5-62 个月), 3 年 OS 和 PFS 率分别为 82% 和 58%。没有与治疗有关的死亡。
【研究结论】
在中国,对老年 DLBCL 患者进行一个简单的 CGA,可能可以有效指导其临床治疗策略。
3. 大于 80 岁老年 DLBCL 患者的治疗策略(利妥昔单抗联合蒽环类化疗)
【研究目的】
目前对于体弱及伴合并症老年 DLBCL 患者的合适治疗方案的选择很少,在真实世界中,以蒽环类药物为基础的化疗方案(anthracycline-based chemotherapy,CHT-A) 可以减少毒性或者可以给患者提供较低强度的化疗方案。该项观察性多中心研究的目的是前瞻性评估 80 岁以上 DLBCL 的患者的临床特征,治疗方案和结局,并比较不同化疗方案的疗效和安全性。
【研究方法】
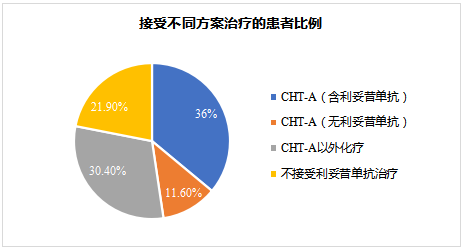
1999 年至 2014 年,共有 4473 名新诊断为 DLBCL 的患者(中位年龄为 64 岁),80 岁以上的患者有 420 名(9.4%)。将 372 例具有完整医疗记录和随访记录的患者纳入最终分析,其中 319 例患者接受了化疗(85.8%),152 例患者(40.8%)接受了一线 CHT-A 方案(30.9% 患者接受了含有利妥昔单抗的 CHT-A 治疗, 9.9% 接受无利妥昔单抗的 CHT-A 治疗)。其余 167 例(44.9%)患者接受了 CHT-A 方案以外的治疗(n = 97; 26.1%)或不接受(n = 70; 18.8%)利妥昔单抗治疗。该研究是注册观察研究 NiHiL(NCT03199066)的一部分。
【研究结果】
整个队列的中位随访时间为 42 个月,在 372 名老年 DLBCL 患者中,(中位年龄 82 岁;年龄范围 80-94),临床晚期(III-IV)占 45.1%,PS 得分 2-4 占 49.2%,IPI 评分 3-5 占 52.5%。与其他患者相比,接受 CHT-A 和利妥昔单抗治疗的患者年龄明显较小(中位年龄 81 岁 vs. 82 岁,p = 0.001),并且具有更好的体能状态(PS ≥ 2,34.8%vs. 50.3%;p = 0.035),未发现其他基线特征差异。
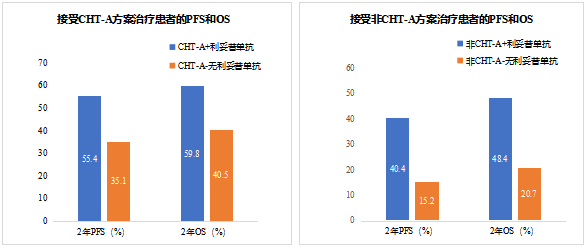
利妥昔单抗在 CHT-A 方案中的使用率(75.7%)显著高于非 CHT-A 方案(58.1%),并且随时间增长,利妥昔单抗使用频率增加,最近 4 年观察发现,在 CHT-A 中达到 94.9%,而在非 CHT-A 中为 73.8%。利妥昔单抗加入可显著改善 CHT-A 方案治疗的 PFS 和 OS(2 年 PFS 55.4% vs. 35.1%, HR 0.66,p = 0.037; 2 年 OS 59.8% vs. 40.5%,HR 0.68 ,p = 0.064)以及非 CHT-A 方案的 PFS 和 OS(2 年 PFS 40.4% vs. 15.2%,HR 0.55,p<0.001; 2 年 OS 48.4% vs. 20.7%; HR 0.59;p = 0.002)。与其他方案相比,使用 CHT-A 和利妥昔单抗治疗患者的 CR 率较高,2 年 PFS 率较高(55.4% vs. 27.5%,HR 0.57,p <0.001),2 年 OS 也较高(59.8% vs. 59.8%,HR 0.59, p<0.001)。
【研究结论】
在真实世界中,有必要评估 80 岁以上 DLBCL 患者的的治疗耐受性。 对于健康老年患者,可以从 CHT-A 化疗联合利妥昔单抗的标准治疗中获益;对于不适合使用蒽环类药物治疗的体弱患者,可能会从其他非 CHT-A 化疗联合利妥昔单抗治疗中获益。
参考文献:
1. D. Sparksman,et al. 2020 EHA Abstract PB2231
2. J.-F. Bai,et al.2020 EHA Abstract PB2258
3. P. Vodicka,et al. 2020 EHA Abstract EP1228
